浙江大学生命科学研究院汪方炜实验室在The EMBO Journal杂志在线发表了题为“A non-canonical role of the inner kinetochore in regulating sister-chromatid cohesion at centromeres”的研究论文。该研究发现了染色体内层动粒(inner kinetochore)通过直接结合黏连蛋白复合体(cohesin)调控姐妹染色单体黏连(sister-chromatid cohesion)的非经典功能,并阐明了其作用机理。
有丝分裂是真核生物体细胞分裂的基本形式,也是生长发育和组织器官稳态维持的根本基础。有丝分裂通过将自我复制的姐妹染色单体平均分配至两个子细胞中,实现遗传物质由亲代细胞向子代细胞的精确传递。该过程中发生的微小差错都有可能造成子代细胞染色体数目和结构异常,进而促进肿瘤的发生与发展。据估算,一个成人体内每天约有数千亿个细胞在进行着有丝分裂,因此细胞必须拥有一套非常精确的控制系统,才能最大程度地保证在每一次有丝分裂过程中染色体都能正确分离。这套控制系统在分子水平上的运作机制还很不清楚。
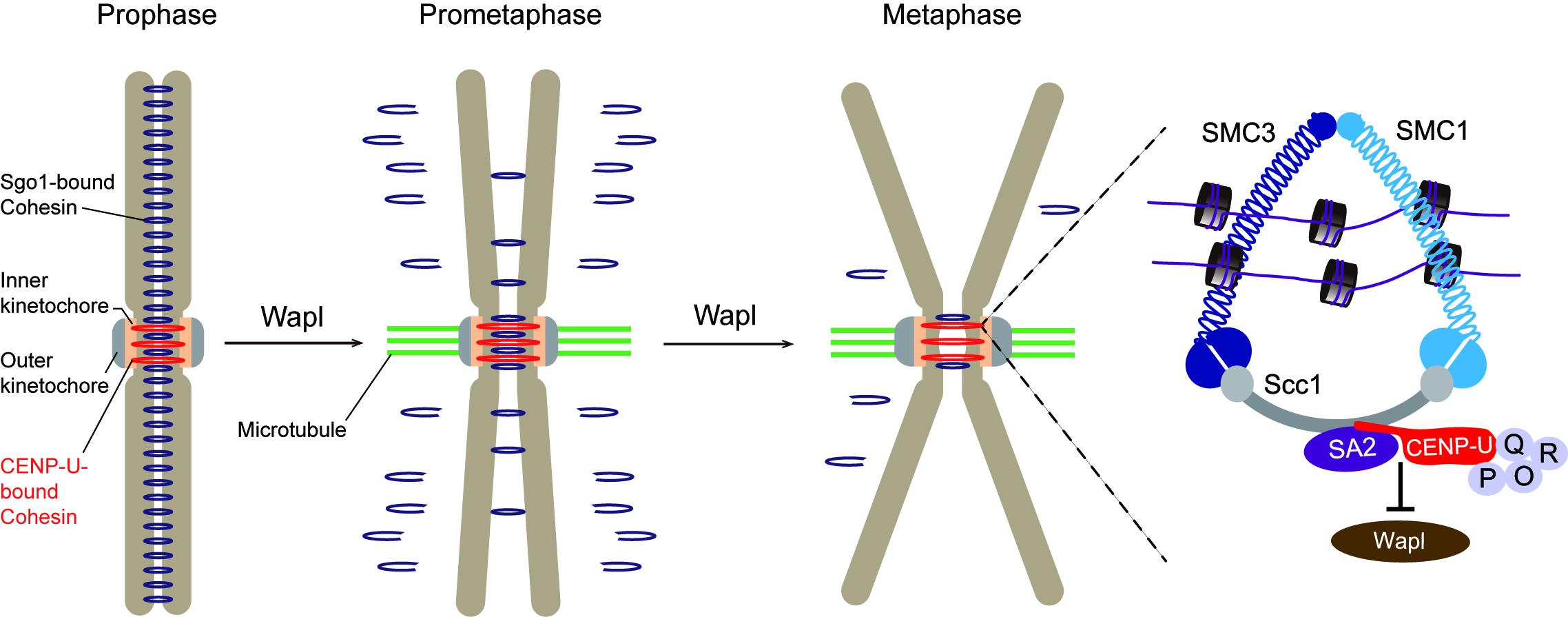
这项研究发现,敲低内层动粒CENP-OPQUR复合体的CENP-U亚基会导致姐妹染色单体在着丝粒区的黏连变弱。蛋白互作实验和质谱分析发现CENP-U可以结合黏连蛋白复合体,而且它们之间的结合依赖于黏连蛋白复合体的核心亚基Scc1和SA2,而非SMC1和SMC3。蛋白复合体的体外重构和互作实验进一步确定,CENP-U的氨基端和羧基端可以分别结合Scc1-SA2亚复合物和CENP-OPQR亚复合物。合作者华中科技大学贺晓静教授通过CENP-U肽段与Scc1-SA2亚复合物的蛋白共结晶实验,解析了CENP-U氨基端的FDF基序结合Scc1-SA2互作界面的结构基础。
功能研究发现,将CENP-U的FDF基序突变为ADA后,不仅破坏了CENP-OPQUR复合体与黏连蛋白复合体的结合,还使得姐妹染色单体黏连变弱。机理研究发现,敲低黏连蛋白的调节亚基Wapl使得姐妹染色单体黏连不再依赖于CENP-U,不能结合CENP-U的Scc1-SA2突变体也部分失去了结合Wapl的能力,而且CENP-U能竞争性地排斥Wapl结合Scc1-SA2亚复合物,说明CENP-U通过抑制Wapl的功能促进姐妹染色单体黏连。
以上结果说明,内层动粒CENP-OPQUR复合体通过其CENP-U亚基的FDF基序直接结合黏连蛋白复合体中Scc1-SA2亚复合物的互作界面,抑制Wapl通过结合Scc1-SA2界面移除着丝粒区黏连蛋白的活性,进而实现对姐妹染色单体黏连的保护作用。
内层动粒最广为人知的功能是连接着丝粒染色质和外层动粒,纺锤体微管通过附着于外层动粒从而牵引染色体移动。这项研究意外地发现内层动粒可通过直接结合黏连蛋白调控姐妹染色单体黏连,不仅揭示了内层动粒作为黏连蛋白受体分子的非经典功能,还阐明了染色体分离控制系统在调控着丝粒黏连这一关键环节中的分子机制。
黏连蛋白环介导姐妹染色单体黏连的确切机制目前还很不清楚。英国牛津大学生化系的Kim Nasmyth实验室近期报道,姐妹染色单体是由单个黏连蛋白环介导的(Ochs F et al., Science, 2024, PMID: 38452070)。然而,有丝分裂中期姐妹染色单体内层动粒的平均间距可达750纳米,约为黏连蛋白环直径的15倍,提示结合于内层动粒的黏连蛋白可能还会以多环串联的方式介导姐妹染色单体黏连。此外,黏连蛋白还在介导染色质环形成中发挥重要作用,内层动粒区的黏连蛋白是否调控着丝粒区染色质的高级结构,还有待探究。
汪方炜教授、颜海燕副教授和贺晓静教授为论文共同通讯作者,浙江大学生命科学研究院颜璐(2020级直博生)、袁雪颖(2021级博士生)以及华中科技大学刘明洁博士为共同第一作者,浙江大学附属妇产科医院吕卫国教授和陈亲富研究员等也有重要贡献。该研究受国家自然科学基金、国家重点研发计划、浙江省自然科学基金、浙江大学生命科学研究院创新项目等资助。
